სტატინების ეფექტიანობა და უსაფრთხოება – მტკიცებულებათა ინტერპრეტაცია
მთარგმნელი: ნათია ვაშაყმაძე, ენდოკრინოლოგი
სტატიის სრულად სანახავად გახსენი სტატიის პდფ ვერსია
მოკლე მიმოხილვა
კლინიცისტებს, პაციენტებსა და საზოგადოებას ხშირად უჭირთ გადაწყვეტა, გამოიყენონ თუ არა სტატინები კორონარული შეტევებისა და ინსულტის საპრევენციოდ. ეს სტატია ხსნის, თუ როგორ ვისარგებლოთ რანდომიზებული კონტროლირებული კვლევებით მიღებულ მტკიცებულებებზე დაფუზნებული სარწმუნო ინფორმაციით სტატინების ეფექტიანობისა და უსაფრთხოების შესახებ. სტატიაში განხილულია ზოგადი სტერეოტიპების შედეგად მათი გამოყენების შეზღუდვა იმ პაციენტებთან, რომელთაც აუცილებლად სჭირდებათ ეს პრეპარატები. აღნიშნული, ასევე, აფერხებს ახალი ინფორმაციის მიღებას სხვა წყაროებიდან, სადაც უტყუარი მტკიცებულებაა მათი ეფექტიანობისა და უსაფრთხოების შესახებ. უამრავი მტკიცებულება არსებობს რანდომიზებული კვლევებიდან, რომ უწყვეტი მიღებისას სტატინები პირველი წლის შემდეგ ამცირებს ვასკულარული დიდი მოვლენების (მაგ., კორონარული სიკვდილობა, ან მიოკარდიუმის ინფარქტი, ინსულტი, კორონარული არტერიების რევასკულარიზაციის პროცედურა) რისკს 1/4-ით LDL-ქოლესტეროლის (დაბალი სიმკვრივის ლიპოპროტეინის) ყოველი 1 მმოლი/ლ-ით შემცირებით ყოველი 1 წლის მანძილზე. სტატინების აბსოლუტური სარგებელი დამოკიდებულია ინდივიდის ოკლუზიური ვასკულარული მოვლენების (ინფარქტი, ან ინსულტი) განვითარების აბსოლუტურ რისკზე, ასევე, სტატინების გამოყენებით LDL ქოლესტეროლის აბსოლუტურ შემცირებაზე. მაგ., LDL ქოლესტეროლის შემცირება 2 მმოლი/ლ-ით (77 მგ/დლ-ით) ეფექტიანი, იაფი სტატინებით (მაგ., ატორვასტატინი 40 მგ დღეში) 5 წლის მანძილზე 10 000-დან დაიცავს 1000 პაციენტს ინფარქტისა და ინსულტის განვითარებისგან (ე.ი. აბსოლუტური რისკი შემცირდება 10%-ით). ეს ეხება პაციენტებს, რომლებსაც უკვე გადატანილი აქვთ კარდიოვასკულარული შემთხვევა, ანუ ეს არის სტატინების როლი ათეროსკლეროზული კარდიოვასკულარული პრობლემის მეორეულ პრევენციაში. ხოლო პაციენტებში, რომლებსაც ჯერ არ გადაუტანიათ ინფარქტი, ან/და ინსულტი და სტატინებს იღებენ პირველადი პრევენციისთვის, აბსოლუტური რისკი 5%-ით მცირდება, ანუ 10 000-დან 500-ს პაციენტს არ დაემართება ინფარქტი, ან ინსულტი. ნანახია, რომ სტატინებით თერაპია ამცირებს ვასკულარული დაავადების რისკს ყოველწლიურად და კიდევ უფრო მეტად, თუ მათ მიღებას განაგრძობენ, ამდენად, რაც უფრო ხანგრძლივია სტატინებით მკურნალობა სარგებელიც ნარჩუნდება დიდი ხნის მანძილზე. სტატინებით ხანგრძლივი თერაპიის სერიოზული გვერდითი ეფექტია მიოპათია (განისაზღვრება როგორც კუნთების ტკივილი, ან კუნთების სისუსტე, რასაც ახლავს სისხლში საერთო კრეატინკინაზის მომატება), შაქრიანი დიაბეტის განვითარება და, შესაძლოა, ჰემორაგიული ინსულტი. ჩვეულებრივ, ეფექტიანი რეჟიმით (მაგ., 40 მგ ატორვასტატინი) 5 წლის მანძილზე 10 000 პაციენტის მკურნალობის შედეგად შეიძლება განვითარდეს მიოპათიის 5 შემთხვევა (რაც სტატინებით თერაპიის გაგრძელების შემთხვევაში შეიძლება პროგრესირდეს უფრო სერიოზულ გართულებად, ე.წ. რაბდომიოლიზი), ახლად განვითარებული დიაბეტის 50-100 შემთხვევა და ჰემორაგიული ინსულტის 5-10 შემთხვევა. 5 წლიანი მკურნალობის ფონზე, სტატინებით თერაპიამ შეიძლება გამოიწვიოს სიმპტომური გვერდითი ეფექტები, მაგ., კუნთების ტკივილი და სისუსტე 10 000-დან 50-100 შემთხვევაში (ე.ი. 0,5-1%). თუმცა, პლაცებოთი კონტროლირებული რანდომიზებული კვლევებით ძალიან მკაფიოდ გამოჩნდა, რომ თითქმის არც ერთი სიმპტომური გვერდითი ეფექტი, რომელიც „რუტინულად“ ახლდა სტატინებით თერაპიას, სრულებითაც არ არის სტატინებით გამოწვეული და, პრაქტიკულად იგივე სიხშირით განვითარდა პლაცებოს ჯგუფშიც. შესაბამისად, სიმპტომური გვერდითი ეფექტები არ იყო გამოწვეული სტატინების გამოყენებით. სტატინები საკმაოდ ძველი და ერთ-ერთი ყველაზე კარგად შესწავლილი პრეპარატების ჯგუფია. უამრავი მტკიცებულებაა დაგროვილი მრავალრიცხოვანი რანდომიზებული, კონტროლირებული კვლევიდან, რომლებიც მიგვანიშნებს, რომ ძალზე ნაკლებ სავარაუდოა, რომ მომავალში რამე სახის სერიოზული ახალი გვერდითი ეფექტი აღმოაჩინონ. შესაბამისად, ნაკლებად მოსალოდნელია, რომ რამე ისეთი გამოვლინდეს, რომელიც ძირეულად შეცვლის სტატინების სარგებელი/რისკის ბალანსს. გასაკვირია, საიდანაა გადაჭარბებული შიში და სტერეოტიპები სტატინების გვერდითი ეფექტების შესახებ, რაც დღემდე ხელს უშლის ექიმებსა და პაციენტებსსტატინების სრულფასოვნად გამოყენებაში გულ-სისხლძარღვთა დაავადების განვითარების მაღალი რისკის დროს, ამით აირიდონ ინფარქტისა და ინსულტის ახალი შემთხვევები და პაციენტები დაიცვან მძიმე და, ზოგ შემთხვევაში, ლეტალური გამოსავლებისგან. სტატინებით გამოწვეული მიოპათიისა და კუნთებთან დაკავშირებული სიმპტომების იშვიათი შემთხვევები დაუყოვნებლივ ქრება სტატინების შეჩერებისას, მაშინ, როცა გულის შეტევებისა და ინსულტების შედეგები მათთვის, ვისაც შეუჩერდა სტატინები, სტერეოტიპებისა და ცრუ შეხედულებების გამო, შესაძლოა, დამღუპველი იყოს.
შესავალი
თანამედროვე სამკურნალო საშუალებების საჭიროებისამებრ გამოყენება გულ-სისხლძარღვთა დაავადებების დიდი პროცენტით არიდების საშუალებას იძლევა. თუმცა, მართებულად გამოყენება უნდა ეყრდნობოდეს სარწმუნო მონაცემებს ეფექტიანობისა და უსაფრთხოების შესახებ, ასევე, მათ სწორ გააზრებასა და ინტერპრეტაციას.
LDL ქოლესტეროლის შემცირების პოტენციური სარგებელი და ზიანი
კავშირი LDL ქოლესტეროლის დონესა და ვასკულარულ დაავადებებს შორის
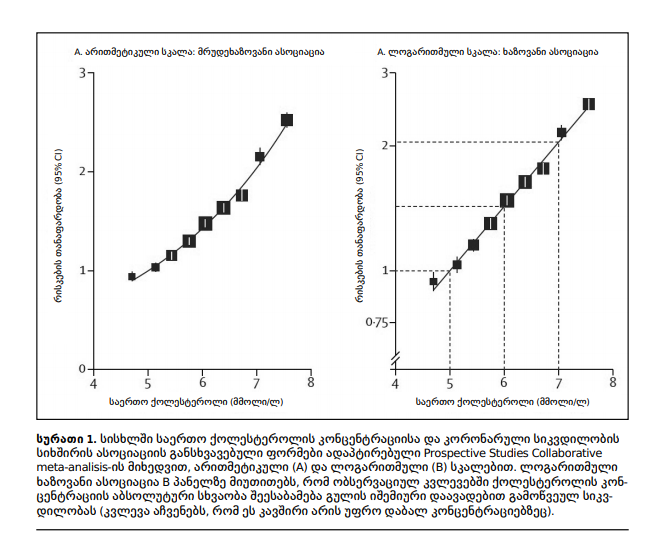
ობსერვაციული ეპიდემიოლოგიური კვლევები აჩვენებს, რომ სხვადასხვა პოპულაციისთვის არსებობს უწყვეტი დადებითი კავშირი სისხლში LDL ქოლესტეროლი დონესა და გულის კორონარულ მოვლენებს შორის. მოცემული კვლევების მიხედვით ვერ იქნა ნანახი LDL ქოლესტეროლის ისეთი დაბალი დონე, რომლის შემდგომი დაქვეითებაც აღარ შეამცირებდა კარდიოვასკულარულ რისკებს. რაც მეტია LDL ქოლესტეროლის დონე სისხლში, მით მაღალია ათეროსკლეროზული კარდიოვასკულარული დაავადებების განვითარების რისკი. არსებობს პირდაპირი კავშირი სისხლში LDL ქოლესტეროლისდონესა და კარდიოვასკულარულ რისკებს შორის (იხ. სურათი1).
სურათი 1. სისხლში საერთო ქოლესტეროლის კონცენტრაციისა და კორონარული სიკვდილობის სიხშირის ასოციაციის განსხვავებული ფორმები ადაპტირებული Prospective Studies Collaborative meta-analisis-ის მიხედვით, არითმეტიკული (A) და ლოგარითმული (B) სკალებით. Log – ხაზოვანი ასოციაცია B პანელზე მიუთითებს, რომ ობსერვაციულ კვლევებში ქოლესტეროლის კონცენტრაციის აბსოლუტური სხვაობა შეესაბამება გულის იშემიური დაავადებით გამოწვეულ სიკვდილობას (კვლავა აჩვენებს, რომ ეს კავშირი არის უფრო დაბალ კონცენტრაციებზეც).
LDL ქოლესტეროლის საწყისი დონის მიუხედავად, LDL ქოლესტეროლის თითოეული მმოლი/ლ-ით დაქვეითება პროპორციულად ამცირებს გულ-სისხლძარღვთა დაავადების რისკებს (იმ მოსაზრების პარალელურად, რომ სტატინების მიერ კარდიოვასკულარული რისკის შემცირება მიიღწევა LDL ქოლესტეროლის დაქვეითებისგან დამოუკიდებელი მექანიზმებითაც); უფრო მეტიც, პაციენტებს რომლებსაც აქვთ ერთნაირი ASCVD რისკები, მაგრამ განსხვავებული აქვთ სისხლში საწყისი LDL ქოლესტეროლის დონეები, აბსოლუტური რისკის შემცირება მსგავსი იქნება LDL ქოლესტეროლის თითოეული მმოლი/ლ-ზე შემცირების საპასუხოდ. ამ ეპიდემიოლოგიური მონაცემების სიზუსტე დაადასტურა რანდომიზებულმა პლაცებო-კონტროლირებულმა კვლევებმა და ახალი გაიდლაინები უკვე ფოკუსირდებიან პაციენტების ათეროსკლეროზულ დაავადებასთან დაკავშირებული მოვლენების განვითარების ინდივიდუალურ რისკებზე და არა მხოლოდ, სისხლში LDL ქოლესტეროლის დონეზე.
რამდენად უსაფრთხოა სისხლში LDL ქოლესტეროლის დონის დაქვეითება და LDL ქოლესტეროლის რა მაჩვენებლის ქვემოთ ჩამოწევა არის საშიში, ან საზიანო? პასუხი ბუნებრივ მოვლენებში ვეძებოთ: არსებობენ ინდივიდები, რომლებსაც გენეტიკური მუტაციის შედეგად სისხლში LDL ქოლესტეროლის ძალიან დაბალი შემცველობა აქვთ. ყველა მიზეზის გათვალისწინებით, ასეთი ინდივიდების სიკვდილობა შედარებით დაბალია, ვიდრე ზოგად პოპულაციაში, მათ შორის ძალიან ასაკოვან, >90 წლის ასაკის, ინდივიდთა შემთხვევებშიც კი. ამდენად დღეისთვის დაუდგენელია LDL ქოლესტეროლის ქვედა ზღვარი, რომლის შემდგომი დაქვეითებაც იქნებოდა საზიანო, ან არ მოგვცემდა გულ-სისხლძარღვთა დაავადების რისკის შემდგომ შემცირებას.
მიზეზ-შედეგობრივი კავშირი LDL ქოლესტეროლის დონესა და კარდიოვასკულარულ დაავადებას შორის
არსებობს არა მხოლოდ ეპიდემიოლოგიური და რანდომიზებული კვლევები, რომლებიც LDL ქოლესტეროლის დონესა და გულ-სისხლძარღვთა დაავადებებს შორის მიზეზ-შედეგობრივ კავშირს ადასტურებს, არამედ ცხოველებზე ჩატარებული ექსპერიმენტული კვლევებიც, სადაც ნაჩვენებია, რომ დიეტა, რომელიც იწვევს სისხლში LDL ქოლესტეროლის დონის მატებას, ზრდის ათეროსკლეროზულ დაავადების განვითარების ალბათბას, ხოლო ჰიპოლიპიდემიური (რედ. შენიშვნა) დიეტა და პრეპარატები (მათ შორის სტატინები) ამცირებენ ათეროსკლეროზული დაავადებისა და მასთან დაკავშირებული მოვლენების გამოვლენის სიხშირეს. გენეტიკური დაავადებები ინდივიდებში (მაგ., LDL რეცეპტორების მუტაცია), რომლებიც იწვევს სისხლში LDL ქოლესტეროლის მნიშვნელოვან მატებას, დაკავშირებულია ათეროსკლეროზული კარდიოვასკულარული დაავადების ბევრად გაზრდილ სიხშირესთან, უფრო მეტიც, ეს დაავადებები (მაგ., ოჯახური ჰიპერქოლესტეროლემია) წარმოადგენს დოზაზე დამოკიდებული ეფექტის ნათელ მაგალითს, სადაც ინდივიდებს, რომლებსაც გენეტიკური მუტაცია ორივე მშობლისგან გადაეცათ და აქვთ ჰომოზიგოტური ოჯახური ჰიპერქოლესტეროლემია, LDL ქოლესტეროლის დონე სისხლში საშუალოდ – 13 მმოლი/ლ-ზეა და კორონარული არტერიების დაავადება უვითარდებათ 20 წლამდე ასაკში. მაშინ, როცა მუტაცია თუ გადაეცემათ მხოლოდ ერთი მშობლისგან და ვითარდება ჰეტეროზიგოტური ოჯახური ჰიპერქოლესტეროლემია, LDL ქოლესტეროლის საშუალო დონე სისხლში არის 8 მმოლი/ლ და გულის შეტევები ვითარდება უფრო მოგვიანებით, შუახნის ასაკში. ასევე, არის გენეტიკური მუტაციები, რომლებიც იწვევს სისხლში LDL ქოლესტეროლის დონის მსუბუქ მომატებას და ასეთ პაციენტებს ზოგად პოპულაციასთან შედარებით გაზრდილი აქვთ ინფარქტებისა და ინსულტების სიხშირე, თუმცა, უფრო მოგვიანებით ასაკში. ეს მონაცემები კიდევ ერთხელ ცხადყოფს გულ-სისხლძარღვთა პათოლოგიით ავადობასა და სიკვდილობაზე LDL ქოლესტეროლის კონცენტრაციის გავლენას.
სტატინებით თერაპიის ფონზე, LDL ქოლესტეროლის დონის დაქვეითების დადასტურებული სარგებელი
სტატინების აღმოჩენამდე, რანდომიზებული კონტროლირებული კვლევების მეტა-ანალიზების მიხედვით, ჰიპოლიპიდემიურმა დიეტებმა, წამლებმა და ბარიატრიულმა ქირურგიამ, წლების მანძილზე, LDL ქოლესტეროლის შემცირების პარალელურად, შეამცირა არაფატალური ინფარქტებისა და ფატალური კორონარული შემთხვევების სიხშირე. თუმცა, იყო მოსაზრება, რომ ამ დადებითი ეფექტების საპირწონედ იზრდებოდა არაკორონარული სიკვდილი და სიმსივნეები, რის გამოც LDL ქოლესტეროლის დამაქვეითებელი თერაპიის სარგებელი საეჭვო იყო. სტატინებით თერაპიის განვითარებამ, რასაც ყველა მანამდე არსებულ მეთოდთან შედარებით შეუძლია LDL ქოლესტეროლის კონცენტრაციის უფრო მძლავრი დაქვეითება, მოგვცა ნათელი მტკიცებულება იმისა, თუ რა დადებით გავლენას ახდენს კარდიოვასკულარულ შემთხვევებსა და სიკვდილობაზე LDL ქოლესტეროლის დაქვეითება, ამასთან, გაირკვა იწვევს თუ არა LDL ქოლესტეროლის დაქვეითება გვერდით ეფექტებს, მაგ., ზრდის ავადობასა და სიკვდილობას სხვა მიზეზით, თუ არა.

სტატინების გავლენა LDL ქოლესტეროლის კონცენტრაციაზე
ბოლო 20 წლის მანძილზე, ფართოდ გავრცელდა სტატინებით თერაპია იმ პაციენტებთან, რომლებსაც აქვთ ოკლუზიური ვასკულარული დაავადება, ან სხვადასხვა მიზეზების გამო აღენიშნებათ მაღალი კარდიოვასკულარული რისკი (მაგ., შრატის მაღალი ქოლესტეროლი, ან სხვა რისკის ფაქტორები, როგორებიცაა: შაქრიანი დიაბეტი, ჰიპერტენზია, მწეველობა, ან ასაკი). აღნიშნულმა მიდგომამ გამოიწვია ბევრ პოპულაციაში სისხლში LDL ქოლესტეროლისა და საერთო ქოლესტეროლის კონცენტრაციის კლება.
სტატინებით LDL ქოლესტეროლის პროპორციულ შემცირებაზე გავლენას არ ახდენს LDL ქოლესტეროლის საწყისი დონე, ან პაციენტის სხვა თავისებურებები მაგ., ასაკი, სქესი, ვასკულარული რისკი, გენეტიკური მარკერები. სხვადასხვა სტატინს აქვს სხვადასხვა სიძლიერე, ახალ აგენტებს (მაგ., ატორვასტატინი და როზუვასტატინი) უფრო ძლიერად შეუძლიათ LDL ქოლესტეროლის დაქვეითება, ვიდრე ძველ აგენტებს (მაგ., სიმვასტატინი, პრავასტატინი) (იხ. ცხრილი 3). გამოყენებული სტატინის მიუხედავად, დოზის გაორმაგება ამცირებს LDL ქოლესტეროლის დამატებითი 6%-ით (მაგ., 43% vs 49% შემცირება ატორვასტატინის დღიური 20 მგ და 40 მგ-ებისთვის); ამერიკის კარდიოლოგთა კოლეგია და ამერიკის გულის ასოციაცია, 2013 წლის ჰიპერქოლესტეროლემიის გაიდლაინში, ისევე როგორც ამერიკის კლინიცისტ ენდოკრინოლოგთა ასოციაცია, 2017 წლის დისლიპიდემიის გაიდლაინში, განსაზღვრავს სტატინებით თერაპიის ინტენსივობასა და დოზებს. დაბალი ინტენსივობით სტატინებით თერაპია გულისხმობს LDL ქოლესტეროლის 30%-მდე შემცირებას (მაგ., სიმვასტატინი 10 მგ დღეში), საშუალო ინტენსივობით სტატინებით თერაპია – LDL ქოლესტერინის 30%-50% შემცირებას (მაგ., ატორვასტატინის 10-20 მგ-ის, ან როზუვასტატინის 5-10 მგ-ის შემთხვევაში), ხოლო მაღალი ინტენსივობით სტატინებით თერაპია – LDL ქოლესტეროლის 50%-ით, ან მეტად შემცირებას (მაგ., ატორვასტატინი 40-80 მგ, როზუვასტატინი 20-40 მგ/დღეში). მაღალი ინტენსივობის სტატინებით თერაპიით LDL ქოლესტეროლი, სულ მცირე, ქვეითება 2 მმოლი/ლ-ით ინდივიდებთან, რომლებსაც საწყისი LDL აქვთ ≥4 მმოლი/ლ (ასეთია ევროპისა და ჩრდილოეთ ამერიკის მოსახლეობის ლიპიდური სპექტრის ნახევარზე მეტი სტატინებით თერაპიის გარეშე), ხოლო ინდივიდებში, რომელთა საწყისი LDL არის 2 მმოლი/ლ, მაღალი ინტენსივობით სტატინებით თერაპია LDL ქოლესტეროლის დონეს 1 მმოლი/ლ-ით ამცირებს.
შესაბამისად, რამდენადაც ვასკულარული მოვლენების (ინფარქტი, ინსულტი, რევასკულარიზაცია) სიხშირე მცირდება LDL ქოლესტეროლის შემცირების პროპორციულად, მაღალი ინტენსივობის სტატინებით თერაპია უნდა დაენიშნოთ პაციენტებს არა მხოლოდ სისხლში ქოლესტეროლის დონის მომატებისას, არამედ ათეროსკლეროზული კარდიოვასკულარული დაავადების (ინფარქტი, ინსულტი, რევასკულარიზაციის საჭიროება) განვითარების მაღალი რისკის არსებობის შემთხვევაშიც.
ვასკულარული დიდი მოვლენების შემცირება
ჩამოყალიბდა ქოლესტეროლის მკურნალობის მკვლევართა კოლაბორაცია (The Cholesterol Treatment Trialists’ _ CTT), რომლის მიზანსაც წარმოადგენდა ყველა ჩატარებული რანდომიზებული კონტროლირებული კველევის (რომელთა ხანგრძლივობა იყო >2 წელი და პაციენტების რაოდენობა იყო, სულ მცირე, 1000) ინდივიდუალური პაციენტის მონაცემების გაანალიზება. CTT-ის მეტა-ანალიზის თავდაპირველი მიზანი იყო, შეეფასებინა LDL ქოლესტეროლის შემცირების გავლენა ინფარქტებზე, ინსულტებსა და რევასკულარიზაციებზე სხვადასხვა ტიპის პაციენტებთან, უფრო სარწმუნოდ, ვიდრე შესაძლებელია შეფასებულიყო ნებისმიერი განცალკევებული რანდომიზებული კვლევით. ასევე, CTT-ის მეტა-ანალიზი მიზნად ისახავდა (ადრე არსებული ეჭვების გათვალისწინებით), რომ გაერკვია იწვევდა თუ არა სისხლში LDL ქოლესტეროლის დაქვეითება გვერდით ეფექტებს, არავასკულარული მიზეზით განპირობებულ სიკვდილობასა და სპეციფიკურ სიმსივნეებს. შესაბამისად, ყველა შერჩეულ კვლევაში თითოეულ პაციენტზე მოიძიეს მონაცემები, გაანალიზეს მათი საწყისი მახასიათებლები და, ასევე, ინფორმაცია მიოკარდიუმის ინფარქტის, ინსულტის, კორონარული რევასკულარიზაციის, სიმსივნეებისა და კვლევების მიმდინარეობისას განვითარებული სიკვდილობის მიზეზების შესახებ. საერთო ჯამში, CTT მეტა-ანალიზის მიხედვით, 25 000 დიდი ვასკულარული მოვლენა (განისაზღვრა როგორც კორონარული სიკვდილი, მიოკარდიუმის არაფატალური ინფარქტი, ნებისმიერი ტიპის ინსულტი და კორონარული რევასკულარიზაციის პროცედურა) განვითარდა ჩატარებულ კვლევებში 5 წლის მანძილზე. ამ ვასკულარული მოვლენების პროპორციული შემცირება ნანახი იქნა LDL ქოლესტეროლის აბსოლუტური შემცირების პარალელურად. ნანახი იქნა განსხვავება როგორც სტატინით ნამკურნალებ და არანამკურნალებ ჯგუფებს შორის, ისედაბალი და მაღალი ინტენსივობით ნამკურნალებ ჯგუფებს შორისაც. ჯამში, LDL ქოლესტეროლის 1 მმოლი/ლ-ით შემცირებისას კარდიოვასკულარული რისკები შემცირდა 25%-ით, ხოლო 2 მმოლი/ლ-ით შემცირებისას რისკები, პრაქტიკულად, განახევრდა, რისკების შემდგომი შემცირება შენარჩუნდა თითოეულ წელს, როდესაც პაციენტი უწყვეტად იღებდა სტატინებს. უფრო მეტიც, რისკების კიდევ უფრო მეტად შემცირება, მაგ., 60-70%-ით, იქნა ნანახი LDL ქოლესტეროლის 3-4 მმოლი/ლ-ით შემცირების ფონზე. თუმცა, ეს კლინიკურად მნიშნელოვანია მხოლოდ გარკვეულ შემთხვევებში (მაგ., ოჯახური ჰიპერქოლესტეროლემიის მქონე ინდივიდებში, რომლებსაც აღენიშნებათ ქოლესტეროლის ძალიან მაღალი საწყისი მაჩვენებლები).
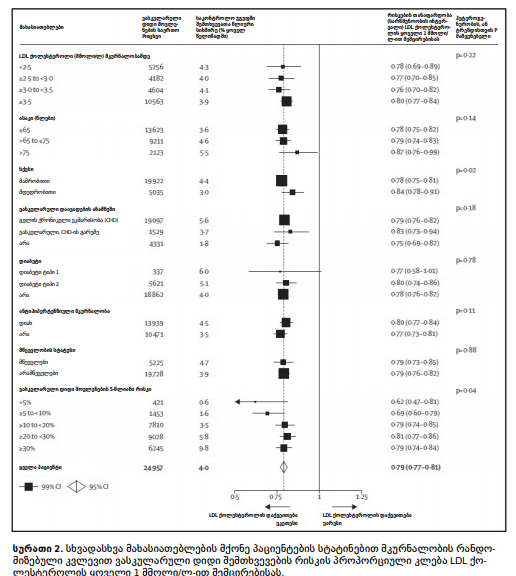
ამ მეტა-ანალიზში, სტატინებით თერაპიამ გამოიწვია LDL ქოლესტეროლისა და ვასკულარული დიდი მოვლენების (მაგ., მიოკარდიუმის არაფატალური ინფარქტი, კორონარული სიკვდილობა, ნებისმიერი სახის ინსულტი და რევასკულარიზაცია) მსგავსი პროპორციული შემცირება. ვასკულარული მოვლენების პროპორციული შემცირება იქნა ნანახი სხვადასხვა ტიპის პაციენტებს შორისაც. მაგ., პაციენტებს პირდაპირპროპორციულად შეუმცირდათ კარდიოვასკულარული მოვლენები LDL ქოლესტეროლის საწყისი დონის მიუხედავად.
სურათი 2. სხვადასხვა მახასიათებლების მქონე პაციენტების სტატინებით მკურნალობის რანდომიზებული კვლევით ვასკულარული დიდი შემთხვევების რისკის პროპორციული კლება LDL ქოლესტეროლის ყოველი 1 მმოლი/ლ-ით შემცირებისას.

ვასკულარული მოვლენების სიხშირე შემცირდა როგორც მეორეული პრევენციის ჯგუფში, ისე იმ პაციენტებთან, სადაც სტატინი იყო დანიშნული პირველადი პრევენციისათვის (მაგ., დიაბეტისა და ჰიპერტენზიის მქონე პაციენტები); თუმცა პროპორციული შემცირება უფრო მეტად იყო გამოხატული დაბალი რისკის მქონე პაციენტებთან. ეს აღმოჩენა თანხვედრაში მოდის Mendelian რანდომიზაციის კვლევებთან, სადაც ნაჩვენებია, რომ გენეტიკური მუტაციის შედეგად სისხლში LDL ქოლესტეროლის დაქვეითება, ათეროსკლეროზის განვითარებამდე, იძლევა რისკის უფრო მეტად შემცირებას, ვიდრე LDL ქოლესტეროლის დაქვეითება ათეროსკლეროზის განვითარების შემდგომ.
ზოგადად, სტატინებით თერაპიის აბსოლუტური სარგებელი დამოკიდებულია პაციენტის ათეროსკლეროზული ვასკულარული მოვლენის განვითარების აბსოლუტურ რისკსა და LDL ქოლესტეროლის აბსოლუტურ დაქვეითებაზე. მაგ., 5 წლის მანძილზე სტატინებით თერაპია თუ LDL ქოლესტეროლის დონეს 2 მმოლი/ლ-ით ამცირებს, მოსალოდნელია მთავარი ვასკულარული შემთხვევების (მიოკარდიუმის არაფატალური ინფარქტი, კორონარული სიკვდილობა, ნებისმიერი სახის ინსულტი და რევასკულარიზაცია) პროფილაქტიკა 1000 პაციენტში (10%) ყოველი 10 000 ნამკურნალები მაღალი რისკის მქონე პაციენტიდან, ხოლო 500 პაციენტში (5%) დაბალი რისკის მქონე 10 000 პაციენტიდან (სურათი 3);
სურათი 3. სხვადასხვა აბსოლუტური რისკის მქონე პაციენტში, 5 წლის მანძილზე სტატინებით მკურნალობის ფონზე, LDL ქოლესტეროლის შემცირებით სისხლძარღვოვანი დიდი შემთხვევების რისკის პროგნოზირებადი აბსულუტური კლება (მკურნალობის 1 წლის შემდეგ).

შესაბამისად, აშკარაა აბსოლუტური სარგებელი LDL ქოლესტეროლის მცირედით შემცირების საპასუხოდაც კი. კვლევების დასრულების შემდგომმა დაკვირვებამ აჩვენა, რომ სტატინებით მიღებული სარგებელი ნარჩუნდება (და, შესაძლოა, იზრდება კიდეც). სტატინების დანიშვნისას პაციენტს ეძლევა რეკომენდაცია, რომ მისი მიღება გაგრძელდეს მუდმივად, სიცოცხლის ბოლომდე. მეტა-ანალიზები აჩვენებს, რომ სტატინებით თერაპია დამატებით ამცირებს გულ-სისხლძარღვთა რისკებს ყოველ შემდგომ წელზე, როდესაც პაციენტი არ წყვეტს მას (სურათი 4).
სურათი 4. სტატინებით მკურნალობისას LDL ქოლესტეროლის 1 მმოლი/ლ-ით შემცირებაზე სისხლძარღვოვანი დიდი შემთხვევების რისკის ყოველწლიური პროპორციული შემცირება რანდომიზებულ კვლევაში, სადაც სტატინებით რეგულარული მკურნალობა შეადარეს სტატინებით არარეგულარულ მკურნალობას.
CTT მეტა-ანალიზის მიხედვით არ იქნა ნანახი რამე სახის უარყოფითი გავლენა სტატინებით თერაპიასა და არავასკულარული მიზეზით სიკვდილობას შორის, უფრო მეტიც, სტატინებით ნამკურნალებ ჯგუფში 15%-ით ნაკლები იყო სიმსივნეებით განპირობებული სიკვდილობა.
სტატინების სხვა დადებითი ეფექტები და სარგებელი
სტატინების ცნობილი და სტანდარტული დადებითი ეფექტების გარდა, რასაც პრეპარატების ეს ჯგუფი იძლევა LDL ქოლესტეროლის დაქვეითებითა და, შესაბამისად, ფატალური და არაფატალური ვასკულარული შემთხვევების პრევენციით, როგორც ჩანს, სტატინებს აქვს დამატებითი დადებითი ეფექტები სხვა მდგომარეობებზე (სავარაუდოდ, მექანიზმებით, რომლებიც არ უკავშირდება სისხლში ქოლესტეროლის დაქვეითებას). მაგ., ნანახია, რომ სტატინები ანახევრებს ღრმა ვენების თრომბოზების და ფილტვის ემბოლიის შემთხვევებს, ცალკეულ ფართომასშტაბიან რანდომიზებულ კვლევებში. თუმცა, ეს შედეგები არ დადასტურდა სხვა რანდომიზებული კვლევებით. ასევე, რამდენიმე მცირემასშტაბიან რანდომიზებულ კვლევაში, სტატინების პერიოპერაციულ პერიოდში გამოყენებით განახევრდა წინაგულთა პოსტოპერაციული ფიბრილაციის სიხშირე . თუმცა, ამ შეფასებისთვის დიდი რანდომიზებული კვლევა არ ჩატარებულა. ასევე, სტატინების გამოყენება თითქოს ასოცირებული იყო ისეთი მდგომარეობების შემცირებასთან, როგორიცაა, ინფექციები, ფილტვის ქრონიკული ობსტრუქციული დაავადება, მწვავე რესპირაციული დისტრეს სინდრომი, თუმცა, შემდგომში ეს მონაცემები მტკიცედ უარყო ადეკვატური ზომის რანდომიზებულმა კვლევებმა.
შეჯამების სახით შეიძლება ითქვას, რომ LDL ქოლესტეროლის სტატინებით შემცირება დადასტურებულად აქვეითებს გულ-სისხლძარღვთა როგორც არაფატალური, ისე ფატალური მოვლენების სიხშირესა და რისკებს. სტატინების აბსოლუტური სარგებელი დამოკიდებულია პაციენტის აბსოლუტურ რისკზე, LDL ქოლესტეროლის შემცირების ხარისხსა და მკურნალობის ხანგრძლივობაზე. მიუხედავად იმისა, რომ სტატინების გამოყენება არ ზრდის არავასკულარული მიზეზით სიკვდილობას, ან სიმსივნეების სიხშირეს, სხვა პოტენციური გვერდითი ეფექტები ყოველთვის გასათვალისწინებელია.
სტატინების დადასტურებული გვერდითი ეფექტები
ყველაზე ხშირი გვერდითი ეფექტები, რომლებიც დადასტურებულად შეიძლება ითქვას, რომ გამოწვეულია სტატინებით, არის მიოპათია და შაქრიანი დიაბეტი, შესაძლო გვერდით მოვლენებში ასევე უნდა განიხილებოდეს ჰემორაგიული ინსულტი. თუმცა, გვერდითი ეფექტების განვითარების აბსოლუტური რისკი მნიშვნელოვნად ნაკლებია, აბსოლუტურ სარგებელთან შედარებით.
სურათი 5. სტატინებით მკურნალობისას ყველაზე გავრცელებული გვერდითი ეფექტების მიმოხილვა.
მიოპათიების შემთხვევების ზრდა
მიოპათია (ზოგჯერ მოიხსენიება როგორც მიოზიტი) განისაზღვრება, როგორც კუნთების ტკივილი, მგრძნობელობის მომატება და სისუსტე, რასაც თან ახლავს სისხლში კრეატინკინაზას საერთო ფრაქციის მნიშვნელოვანი მატება (მაგ., ლაბორატორიული ნორმის ზედა ზღვრიდან >10-ჯერ). რაბდომიოლიზი წარმოადგენს მიოპათიის მძიმე ფორმას, რომლის დროსაც კუნთები იშლება (ჩვეულებრივ, განისაზღვრება როგორც კრეატინკინაზის კონცენტრაციის უფრო გამოხატული მატება), მიოგლობინი გამოთავისუფლდება ცირკულაციაში და, ზოგიერთ შემთხვევაში, თირკმლის ფუნქციის გაუარესებას, ან თირკმლის მწვავე უკმარისობას იწვევს. ჩვეულებრივ, მიოპათია იშვიათია. როგორც ობსერვაციული და რანდომიზებული კვლევების მიხედვით, სტატინების მიღებული რეჟიმები ასოცირებულია მიოპათიის განვითარების დაბალ აბსოლუტურ რისკთან (1 წლის განმავლობაში ყოველ 10 000 პაციენტზე დაახლოებით 1 შემთხვევა, ხოლო რაბდომიოლიზი კიდევ უფრო იშვიათია – 2-3 შემთხვევა ყოველ 100 000 პაციენტზე). მიოპათია, ჩვეულებრივ, უკუვითარდება სტატინით მკურნალობის შეჩერებისას.
მიოპათიის მექანიზმი არ არის ბოლომდე ცნობილი. მიოპათიის რისკი დამოკიდებულია დოზასა და, როგორც ჩანს, მოცირკულირე სტატინის კონცენტრაციაზე (როგორცაჩვენა SLCO1B1 გენის ვარიანტთან ასოციაციამ, ეს გენი აკოდირებს ცილას, რომელიც ამცირებს ყველა სტატინის ტრანსპორტს სისხლიდან ღვიძლში); ცერივასტატინი გატანილია ბაზრიდან მისი გვერდითი ეფექტის, კერძოდ, სხვა სტატინებთან შედარებით მიოპათიების გამოხატულად მაღალი სიხშირის გამო. SEARCH რანდომიზებულ კვლევაში , დღეში 80 მგ სიმვასტატინი ასოცირებული იყო მიოპათიების 10-ჯერად მატებასთან (სულ მცირე, 1 შემთხვევა ყოველ 1000 პაციენტზე, წელიწადში), ვიდრე დღიურად 20 მგ სიმვასტატინის დანიშვნის შემთხვევაში. ამდენად, მაღალი დოზით სიმვასტატინის რუტინულად გამოყენება არ არის რეკომენდებული. მიოპათიის განვითარების სიხშირე უფრო მაღალია ატორვასტატინის მაღალი დოზებით გამოყენების შემთხვევაშიც, თუმცა, აბსოლუტური რისკი კვლავ რჩება ძალიან დაბალი ატორვასტატინის მაქსიმალური დოზით გამოყენების შემთხვევაშიც კი. მიოპათიის რისკი შეიძლება მნიშვნელოვნად გაიზარდოს, როდესაც სტატინებს იყენებენ სხვა ისეთ პრეპარატებთან კომბინაციაში, რომლებიც გავლენას ახდენენ ღვიძლში მათ მეტაბოლიზმზე (განსაკუთრებით, ციტოქრომ P450-ისა და P-გლიკოპროტეინის ინჰიბიტორები, როგორებიცაა ციკლოსპორინები და სოკოს საწინააღმდეგო „აზოლები“). მიოპათიის განვითარების რისკი, აგრეთვე, მატულობს განსაკუთრებული კატეგორიის ინდივიდებში (მაგ., აზიური წარმოშობის პაციენტები, ან პირები, ვისაც აქვთ SLCO1B1 გენის ფუნქციური ვარიანტი). მიოპათიის რისკი შედარებით მსუბუქად აქვთ გაზრდილი პაციენტებს გარკვეული ანტიჰიპერტენზიული თერაპიის ფონზე, ქალებს, >80 წლის ასაკის პირებს, ან დიაბეტის მქონე პაციენტებს .
მიუხედავად მიოპათიის მიზეზ-შედეგობრივი ასოციაციისა, რანდომიზებული კონტროლირებული კვლევები აჩვენებს, რომ სტატინებით თერაპიას მინიმალური გავლენა აქვს კუნთების ტკივილზე (მიალგიასთან), ან სისუსტეზე. ასეთი გვერდითი ეფექტები ხშირად შეიმჩნევა მკურნალობის ფონზე, თუმცა, ნაკლებადაა ასოცირებული სტატინებით თერაპიასთან. ხშირი დებატებია თემაზე სტატინთან ასოცირებული კუნთების სიმპტომები (SAMS) წარმოადგენს თუ არა სტატინების რეალურ გვერდით ეფექტს, თუ nocebo ეფექტს. nocebo ეფექტი გამოწვეულია წამლის მიმართ უარყოფითი მოლოდინებითა და წინასწარი განწყობით, რაც განპირობებულია მედია საშუალებების გავლენით და ექიმების მიერ პაციენტების ინფორმირებით სტატინების შესაძლო გვერდითი ეფექტების შესახებ. The Anglo-Scandinavian Cardiac Outcomes Trial—Lipid-Lowering Arm (ASCOT-LLA) კვლევის მიხედვით, შესაძლოა, სწორედ nocebo ეფექტით აიხსნას სტატინით ინდუცირებული კუნთოვანი სიმპტომების ზრდა ობსერვაციულ კვლევებსა და რეალურ პრაქტიკაში, რანდომიზებულ კლინიკურ კვლევებთან შედარებით.
SAMS-ის შესახებ არსებული საკითხები კლინიცისტებისთვის
- რა არის SAMS? – კუნთების ტკივილი, სისუსტე და დისკომფორტი, ჩვეულებრივ, მოქმედებს სიმეტრიულად და პროქსიმალურად თეძოს, დუნდულოს, წვივისა და ზურგის კუნთებზე, უმეტესად, არ არის დაკავშირებული კრეატინკინაზის მნიშვნელოვან მატებასთან.
- როდის ვლინდება SAMS? – როგორც წესი ვლინდება ადრე (სტატინებით მკურნალობის დაწყებიდან 4-6 კვირაში), სტატინების დოზის გაზრდის შემდეგ, ან იმ პრეპარატთან კომბინაცია, რომელიც გავლენას ახდენს სტატინის მოქმედებაზე.
- ვის აქვს SAMS-ის რისკი? – ძალიან ასაკოვან (>80 წლის ასაკის) პირებს, განსაკუთრებით, ქალებს, სხეულის დაბალი მასის მქონე, ან აზიური წარმოშობის პირებს, რომლებსაც აქვთ კუნთური დარღვევები, ან თანმხლები მდგომარეობები (მაგ., მწვავე ინფექცია, ღვიძლის, ან თირკმლის დისფუნქცია, შაქრიანი დიაბეტი, შიდს-ი), ან იღებენ ისეთ მედიკამენტებს, რომელიც გავლენას ახდენს სტატინის მოქმედებაზე.
- როგორ განსაზღვრავს SAMS-ს EAS-ის (ევროპის ათეროსკლეროზის საზოადოების) კონსენსუსის კომისია? – კუნთისმხრივი სიმპტომების მახასიათებლებით, სტატინებით მკურნალობის დაწყებასა და კუნთისმხრივი სიმპტომების გამოვლენას შორის დროში კავშირით, სტატინებით მკურნალობის შეწყვეტასა და მკურნალობის განახლებისას სიმპტომების კვლავ გამოვლინებით.
- რა განსაზღვრავს SAMS-ის მართვას? – კრეატინკინაზის მატების სიდიდე და პაციენტის გლობალური კარდიოვასკულარული რისკი.
დიაბეტის შემთხვევების ზრდა
JUPITER რანდომიზებული კლინიკური კვლევის მიხედვით, ვასკულარული დაავადების არმქონე 17 802 პაციენტიდან მათ, რომლებიც იღებდნენ როზუვასტატინს 20 მგ დღეში, 2 წლიანი თერაპიის ფონზე, აღენიშნებოდათ HbA1c-ის დონის (5,9% vs 5.8% p=0.001) და დიაბეტის ახალი შემთხვევების მცირედი მატება (3% vs 2.4%; p=0.01), რაც შეესაბამება 25%-იან პროპორციულ ზრდას, პლაცებოსთან შედარებით. , რანდომიზებული კვლევების შედეგების შემდგომი მეტა-ანალიზით გაირკვა, რომ სტატინების სტანდარტული დოზებით გამოყენება ასოცირებულია ახლად გამოვლენილი დიაბეტის განვითარების რისკის 10%-იან ზრდასთან, ხოლო უფრო ინტენსიური თერაპია, როგორიც JUPITER კვლევაში გამოიყენებოდა, დაკავშირებული იყო 10%-იან დამატებით რისკთან. სტატინით ნამკურნალებ ჯგუფში დიაბეტის განვითარების მაღალი რისკი აქვთ პაციენტებს, რომლებსაც დიაბეტის განვითარების რისკის ფაქტორები აღენიშნებათ (მაგ., სიმსუქნე, ჭარბი წონა, ან გლიკოზირებული ჰემოგლობინისა და გლიკემიის ნორმიდან გადახრა). რისკი არ იზრდება მკურნალობის ხანგრძლივობის ზრდასთან ერთად.
გენეტიკური ვარიანტი, რომელიც ამცირებს HMC-CoA რედუქტაზას აქტივობას (რასაც სტატინების ანალოგიური ეფექტი აქვს), ასევე, ასოცირებულია დიაბეტის სიხშირის ზრდასთან. ამის მსგავსად, ოჯახური ჰიპერქოლესტეროლემიის მქონე ინდივიდებთან, ვისაც პლაზმურ მემბრანაზე შემცირებული აქვთ ფუნქციურად სრულყოფილი LDL ქოლესტეროლის რეცეპტორების რაოდენობა (განსხვავებით სტატინების მოქმედებისგან, როდესაც LDL ქოლესტეროლის რეცეპტორების რაოდენობა გაზრდილია), დიაბეტის დიაგნოსტიკა უფრო იშვიათადია, ვიდრე ოჯახური ჰიპერქოლესტეროლემიის არმქონე მათ ნათესავებთან. ბუნების ეს ექსპერიმენტები გვაფიქრებინებს, რომ ასოციაცია სტატინების გამოყენებასა და დიაბეტის განვითარებას შორის მიზეზ-შედეგობრივია, თუმცა, მექანიზმი უცნობია. შესაძლებელია, იგი დაკავშირებული იყოს LDL ქოლესტეროლის უშუალო შემცირებასთან, თუმცა, არსებობს ჰიპოთეზა, LDL რეცეპტორების რაოდენობის ზრდამ (მაგ., სტატინებითა და PCSK9 ინჰიბიტორებით თერაპიისას), შესაძლოა, ხელი შეუწყოს პანკრეასის ბეტა უჯრედებში ქოლესტეროლის დიდი რაოდენობით შესვლას, მათ დაზიანებასა და დიაბეტის განვითარებას.
აქვე აღსანიშნავია, რომ დიაბეტის გახშირების კლინიკური მნიშვნელობა ბოლომდე ნათელი არ არის, განსაკუთრებით, თუ გავითვალისწინებთ, რომ სტატინებით თერაპიის კარდიოვასკულარული სარგებელი მნიშვნელოვნად მაღალია, ვიდრე დიაბეტთან დაკავშირებული ნებისმიერი სახის ავადობა. ახლად გამოვლენილი დიაბეტის სიხშირე პირველადი პრევენციის ჯგუფში იყო დაახლოებით 1% წელიწადში. ამდენად, სტატინებით თერაპიისას აბსოლუტური სიხშირე არის 10-20 შემთხვევა 10 000 პაციენტზე წელიწადში. თუკი მივიღებთ მხედველობაში იმ ფაქტს, რომ დიაბეტი აორმაგებს კარდიოვასკულარულ რისკებს (ვგულისხმობთ, სპონტანურად განვითარებული დიაბეტის შემთხვევას) ეს მაჩვენებლები საყურადღებოა, თუმცა, იმ პაციენტებთან, რომლებსაც დიაბეტი სტატინებით თერაპიის ფონზე ჩამოუყალიბდათ, ინფარქტისა და ინსულტის განვითარების სიხშირე არ იზრდება და ისეთივეა, როგორიც დიაბეტის გარეშე იქნებოდა. 5 წლის მანძილზე სტატინებით თერაპია 10 000 პაციენტზე 150-300 სისხლძარღვოვანი მოვლენის პრევენციას იწვევს. აბსოლუტური სარგებელი კიდევ უფრო დიდია მაღალი რისკის მქონე პაციენტებთან (მათ შორის იმათთან, რომლებსაც უკვე აქვთ დიაბეტი – სურათები 1 და 5); ერთ-ერთი მეტა-ანალიზის მიხედვით, 4 წლის მანძილზე სტატინით მკურნალობა იწვევს 255 პაციენტიდან დიაბეტის 1 შემთხვევას. 4 წლის მანძილზე 255 პაციენტიდან დიაბეტის 1 შემთხვევის საპირწონედ კი 9 ინფარქტისა და ინსულტის პრევენცია მოხდება. აშკარაა, რომ სტატინების სარგებელი მნიშვნელოვნად აღემატება გვერდითი ეფექტების რისკებს.
სამახსოვრო
- რანდომიზებული კლინიკური და გენეტიკური კვლევების მიხედვით სტატინებით თერაპია ასოცირებულია შაქრიანი დიაბეტის ახალი შემთხვევების მცირე ზრდასთან. 1 წლის მანძილზე სტატინებით თერაპიისას იზრდება შაქრიანი დიაბეტის ახალი შემთხვევის გამოვლენის სიხშირე და, ამავდროულად, ხდება კარდიოვასკულარული 5 მოვლენის (ინფარქტი და ინსულტი) თავიდან არიდება;
- პირებს, რომლებსაც აქვთ მეტაბოლური სინდრომის მახასიათებლები, ან პრედიაბეტი, მნიშვნელოვნად მაღალი აქვთ სტატინებით ინდუცირებული დიაბეტის განვითარების რისკი ვიდრე პირებს მეტაბოლური სინდრომის გარეშე. თუმცაღა, ამ მდგომარეობის შაქრიან დიაბეტში გადასვლა სტატინების გარეშეც მაღალია;
- პაციენტებს უნდა განემარტოთ, რომ, ინფარქტისა და ინსულტის შემცირების თვალსაზრისით, სტატინებით განპირობებული სარგებელი მნიშნელოვნად აღემატება გლუკოზის ცვლის დარღვევის პოტენციურ რისკს, განსაკუთრებით, მეტაბოლური სინდრომისა და მომატაბული გლიკოზირებული ჰემოგლობინის მქონე პირებთან, რომლებსაც ძალიან მაღალი აქვთ გულ-სისხლძარღვთა დაავადებების განვითარების ალბათობა.
ჰემორაგიული ინსულტების შესაძლო ზრდა
ობსერვაციული კვლევების მიხედვით, სისხლში ქოლესტეროლის კონცენტრაცია უარყოფითად არის ასოცირებული ჰემორაგიულ ინსულტებთან, განსაკუთრებით, თუ მაღალი არტერიული წნევის ფონზე აღინიშნება ქოლესტეროლი დაბალი კონცენტრაცია. SPARCL რანდომიზებულ კვლევაში, სადაც ჩართული იყო ადრე არსებული ცერებროვასკულარული დაავადების მქონე 4731 პაციენტი, დღეში 80 მგ ატორვასტატინით თერაპიამ არსებითად შეამცირა იშემიური ინსულტის სიხშირე (218 (9,2%) vs 274 (11.6%); p=0.008), თუმცა, დაფიქსირდა ჰემორაგიული ინსულტების შესაძლო ზრდა (55 (2,3%) vs 33 (1.4%); p=0.02). როდესაც ეს შედეგები შეჯერდა სხვა კვლევის შედეგებთან, როგორიცაა მაგ., CTT-ის მიერ ჩატარებული მეტა-ანალიზი, ნანახი იქნა ჰემორაგიული ინსულტების სიხშირის 21%-ით პროპორციული ზრდა, LDL ქოლესტეროლის თითოეული მმოლი/ლ-ით შემცირების საპასუხოდ.
ევროპისა და ჩრდილოეთ ამერიკის მოსახლეობაში ეს ნიშნავს ჰემორაგიული ინსულტის 5-10 შემთხვევას ყოველ 10 000 პაციენტზე, რომლებსაც LDL ქოლესტეროლი 5 წლის მანძილზე სტატინებით თერაპიის შედეგად 1-2 მმოლი/ლ-ით შეუმცირდათ. აბსოლუტური რისკი, შესაძლოა, კიდევ უფრო მეტი იყოს იმ პაციენტებთან, ვისაც უკვე აქვს ცერებროვასკულარული დაავადება, ან აზიელ პაციენტებთან, სადაც ჰემორაგიული ინსულტების სიხშირე ისედაც უფრო მაღალია.
ამ აღმოჩენის შემდეგ ჩატარდა კვლევების მეტა-ანალიზი, რომელიც მოიცავდა 248 391 პაციენტს. რანდომიზებული კლინიკური კვლევების მეტა-ანალიზის მიხედვით არ იქნა ნანახი სტატინებით თერაპიის მქონე პირებთან ჰემორაგიული ინსულტის მნიშვნელოვნად გაზრდილი რისკი (რისკების თანაფარდობა 1.10, 95% CI 0.86–1.41). ასევე, არ იქნა ნანახი განსხვავება კლინიკური შემთხვევებით კონტროლირებულ კვლევებში (RR 0.60,95% CI 0.41–0.88). ამ პაციენტების დამატებითი მეტა-ანალიზის მიხედვით არ იქნა ნანახი ასოციაცია ჰემორაგიული ინსულტის რისკსა და LDL ქოლესტეროლის შემცირებას შორის.
სამახსოვრო
- სტატინებით თერაპია ამცირებს როგორც პირველ, ისე მომდევნო იშემიურ ინსულტებს 15-35%-ით, თითოეული 1 მმოლი/ლ-ით LDL-C ქოლესტეროლის შემცირების საპასუხოდ.
- მართალია, SPARCL-ის თანახმად გამოითქვა მოსაზრება გადატანილი ინსულტის შემდეგ LDL ქოლესტეროლის შემცირების საპასუხოდ ჰემორაგიული ინსულტების მცირედ მატების შესახებ, მაგრამ ეს ფაქტი არ დადასტურდა შემდგომი რანდომიზებული კლინიკური, კოჰორტული და შემთხვევა–კონტროლირებული კვლევების მეტა-ანალიზითა და თანამედროვე მტკიცებულებით.
- სტატინების დოზის ცვლილება, ან კორექცია არ არის ნაჩვენები მათთვის, ვისაც ანამნეზში ცერებროვასკულარული დაავადება აღენიშნება.
თირკმლისმიერი უსაფრთხოება
რადგან სტატინებით თერაპია მსუბუქად ზრდის დიაბეტის განვითარების სიხშირეს, ლოგიკურია ვიმსჯელოთ რა გავლენას ახდენს იგი დიაბეტური მიკროვასკულარული გართულებების სიხშირეზე. 57 რანდომიზებულ კონტროლირებულ კვლევის მეტა-ანალიზის მიხედვით(ჩართული პაციენტების რაოდენობა იყო 140 000 რომლებიც, სულ მცირე, 6 თვის მანძილზე მკურნალობდნენ სტატინებით), სტატინებით თერაპიამ შეანელა გორგლოვანი ფილტრაციის სიჩქარის კლების პროცესი 0,41 მლ/წთ/1,73 მ2-ით წელიწადში (95% CI 0,11–0,70); მეტიც, რანდომიზებული კვლევიდან 5000 პაციენტს საკონტროლო ჯგუფთან შედარებით, სტატინებით თერაპიამ მსუბუქად შეამცირა ალბუმინურია და პროტეინურია. მიუხედავად ამ დადებითი სასარგებლო ეფექტებისა, სტატინების გამოყენება არ ცვლის თირკმლის ქრონიკული დაავადების პროგრესირებასრანდომიზებულ კლინიკურ კვლევებში: სტატინით ნამკურნალები ჯგუფის 1261 პაციენტი (13,5%) საკონტროლო ჯგუფის 1282 პაციენტთან შედარებით (13,6%) (შანსების თანაფარდობა 0,98, 95% CI 0,90–1,07).
კარდიოქირურგიის შემდეგ, პერიოპერაციულად მოკლე პერიოდით სტატინების გამოყენებისას ნანახი იქნა სისხლში კრეატინინის ზრდა, რაც გარკვეულ რანდომიზებულ კონტროლირებულ კვლევებში შეესაბამებოდა თირკმლის მწვავე დაზიანებას, თუმცა, ფართომასშტაბიანი კვლევებით, სადაც სტატინები ხანგრძლივად გამოიყენეს, თირკმლის უკმარისობის შემთხვევების მატება ნანახი არ იქნა. მაგ., SHARP კლინიკურ კვლევაში, , სადაც ჩართულნი იყვნენ სტატინების დაწყებამდე დადგენილი თირკმლის ქრონიკული დაავადების მქონე პირები, თირკმლის ფუნქციის გაუარესება, ან უკმარისობა აღენიშნებოდა პაციენტთა 6,7%-ს, რომლებიც იმყოფებოდნენ თერაპიაზე 20 მგ სიმვასტატინი + 10 მგ ეზეტიმიბი, ხოლო პლაცებოს ჯგუფში – 7,4%-ს. The Heart Protection Study-ის მიხედვით, იმ პაციენტებს შორის, რომლებსაც უკვე ჰქონდა გადატანილი კარდიოვასკულარული პრობლემა, ან ჰქონდათ დიაბეტი, თირკმლის ფუნქციის გაუარესება, ან უკმარისობა აღენიშნა 0,6%-ს, ისევე, როგორც 40 მგ სიმვასტატინით მკურნალობაზე მყოფ ჯგუფში. თირკმლის ფუნქცია შეფასდა სტატინების გამოყენებისას პირველადი პრევენციის მიზნით ჩატარებულ JUPITER კვლევაში; თირკმლის ფუნქციის გაუარესება ნანახი იქნა 20 მგ როზუვასტატინით თერაპიის ჯგუფში 71 პაციენტთან (0,9%), ხოლო პლაცებოს ჯგუფში კი 70 პაციენტთან (0,9%) (რისკების თანაფარდობა 1,01, 95% CI 0,73–1,41).
შესაბამისად, რანდომიზებული კონტროლირებული კვლევებიდან მიღებული მტკიცებულებები არ იძლევა საფუძველს ვიფიქროთ, რომ სტატინებს რამე უარყოფითი გავლენა აქვს თირკმლის ფუნქციაზე (სავარაუდოდ, პერიოპერაციული პერიოდის გარდა) და, პირიქით, გვაჩვენებს, რომ ისინი მსუბუქად აუმჯობესებენ თირკმლის ფუნქციას (თუმცა, ამ მსუბუქი დადებითი ეფექტის კლინიკური მნიშვნელობა დაუზუსტებელია); ასევე, აღსანიშნავია, რომ თუ სტატინებით ინდუცირებული მიოპათიებისას არ შეჩერდა სტატინებით თერაპია, შეიძლება, თირკმლის უკმარისობა გამოიწვიოს. შესაბამისად, ექიმებიც და პაციენტებიც ყურადღებით უნდა იყვნენ და იცოდნენ ამ იშვიათი გართულების შესახებ. აუცილებლად აღსანიშნავია, რომ კუნთისმხრივი სიმპტომები არ უნდა „დაბრალდეს” სტატინებს გადამოწმებისა და ობიექტური მტკიცებულების, მაგ., კრეატინკინაზის საერთო ფრაქციის მნიშვნელოვანი მატების, გარეშე და „უდანაშაულო“ სტატინები დაუსაბუთებლად არ უნდა მოიხსნას/შეჩერდეს.
ბოლო პერიოდში ჩატარებული მეტა-ანალიზები აჩვენებს, რომ სტატინებით თერაპია ამცირებს კარდიოვასკულარულ რისკებს თირკმლის ქრონიკული დაავადების შემთხვევაში, განსაკუთრებით, თირკმლის ფუნქციის მსუბუქი დარღვევისას. აღსანიშნავია, რომ დიალიზზე მყოფ პირებთან სტატინებით თერაპია სარგებელს არ იძლევა. ამდენად, თანამედროვე გაიდლაინები ეყრდნობა რა ამ მონაცემს, რეკომენდაციას უწევს სტატინების აქტიურ გამოყენებას თირკმლის ქრონიკული დაავადების მქონე პირებში, გარდა დიალიზზე მყოფი პაციენტებისა.
სტატინების მაღალი დოზებით თერაპიის ფონზე აღნიშნული მსუბუქი პროტეინურია, რომელიც, მეტწილად, გარდამავალია, არ არის დაკავშირებული თირკმლის ფუნქციის გაუარესებასთან. იგი შესაძლოა გამოწვეული იყოს ალბუმინის ტუბულარული რეაბსორბციის შემცირებით, სტატინების მიერ ფერმენტ HMG-CoA რედუქტაზას ინჰიბიციითა და ენდოციტოზში მონაწილე ცილების პრენილირების დაქვეითებით. ეს ეფექტი, როგორც წესი, იშვიათი და გარდამავალია. რანდომიზებული კლინიკური კვლევების მეტა-ანალიზების მიხედვით, მაგ., 24 კლინიკური კვლევის მეტა-ანალიზით, კვლევაში ჯამურად ჩართული იყო წლების მანძილზე სტატინებით ნამკურნალები >15 000 პაციენტი, არ იქნა ნანახი სერიოზული თირკმლისმიერი ცვლილება. უფრო მეტიც, არსებობს გარკვეული მოსაზრება და კვლევები, რომელთა მიხედვითაც სტატინებს, შესაძლოა, ჰქონდეთ ნეფროპროტექციული მოქმედებაც, თუმცა, ეს ჰიპოთეზა დამატებით კველევას საჭიროებს.
სამახსოვრო
- სტატინებით თერაპია არ არის ასოცირებული თირკმლის ფუნქციის კლინიკურად მნიშვნელოვნად გაუარესებასთან.
- გლომერულური ფილტრაციის მიხედვით დოზის შემცირება შესაძლოა საჭირო იყოს თირკმლის ქრონიკული დაავადების შორეულ სტადიაზე, გარკვეული სტატინებისთვის, მაღალი დოზებით მათი გამოყენების შემთხვევაში.
- სტატინების პროტექციული ეფექტი თირკმლებზე არ არის გამორიცხული, თუმცა, ამ მიმართულებით საჭიროა დამატებით კვლევების ჩატარება.
სტატინები და ღვიძლი
სტატინებით გამოწვეული ღვიძლის იდიოსინკრაზული დაზიანება უკიდურესად იშვიათი ფენომენია, თუმცა, თუ განვითარდა, შესაძლოა, საკმაოდ სერიოზული აღმოჩნდეს. ჩატარებული კვლევების მიხედვით, სტატინებით განპირობებული ღვიძლის დაზიანება, შესაძლოა, წამლით გამოწვეული ჰეპატოტოქსიკურობის 1-3%-ს შეადგენდეს. The United Kingdom General Practice Recearch Database-ის (1997-2006 წ.) მონაცემებით, ღვიძლის ზომიერი და გამოხატული დაზიანება (ბილირუბინი >60 მკმოლი/ლ, ALT, ან AST > 200 ერთ/ლ, ან ALP > 1200 ერთ/ლ) ატორვასტატინით თერაპიისას ნანახი იქნა პაციენტთა მხოლოდ 0,09%-ში vs სიმვასტატინის ფონზე 0,06%-ში. წამალთა გვერდითი ეფექტების მონაცემთა შვედეთის ბაზის მიხედვით, სტატინებით თერაპიის დროს, წამლით განპირობებული ღვიძლის დაზიანება (განისაზღვრება როგორც ტრანსამინაზების მომატება ნორმის ზედა ზღვრიდან ≥5-ჯერ და ტუტე ფოსფატაზის ზრდა ნორმის ზედა ზღვრიდან ≥2) დაფიქსირებულია11,2 შემთხვევა 100 000 პაციენტზე. მიუხედავად 1990 წლიდან სტატინების გამოყენების მნიშვნელოვნად გაზრდისა, FDA-ის გვერდითი ეფექტების აღწერის სისტემის მონაცემთა ბაზას არ აღმოუჩენია სტატინებით ინდუცირებული ღვიძლის ფატალური, ან მძიმე დაზიანების შემთხვევების ზრდა. სტატინით ინდუცირებული ღვიძლის მძიმე დაზიანება უკიდურესად იშვიათია – <2 შემთხვევა 1 მილიონ პაციენტზე წელიწადში. შემთხვევები შეფასდა როგორც შესაძლო, ან სტატინებით თერაპიასთან სავარაუდოდ ასოცირებული. არც ერთი შემთხვევა არ შეფასებულა როგორც ძალზე სავარაუდო, ან სტატინებით თერაპიასთან დადასტურებულად დაკავშირებული. ამერიკის ლიპიდების ეროვნული ასოციაციის ღვიძლისმიერი უსაფრთხოების კომისიის ბოლო განახლების მიხედვით, სტატინებით განპირობებული ჰეპატოტოქსიკურობის აღწერილი შემთხვევები ძალიან იშვიათია. სტატინებით განპირობებული ღვიძლის დაზიანება უნდა იყოს კლასის ეფექტი და, შესაძლოა, განვითარდეს მკურნალობის დაწყებიდან ნებისმიერ დროს. აუტოიმუნური ჰეპატიტი, სავარაუდოდ, სტატინით ინდუცირებული ჰეპატოტოქსიკურობის ყველაზე ხშირი ვარიანტია.
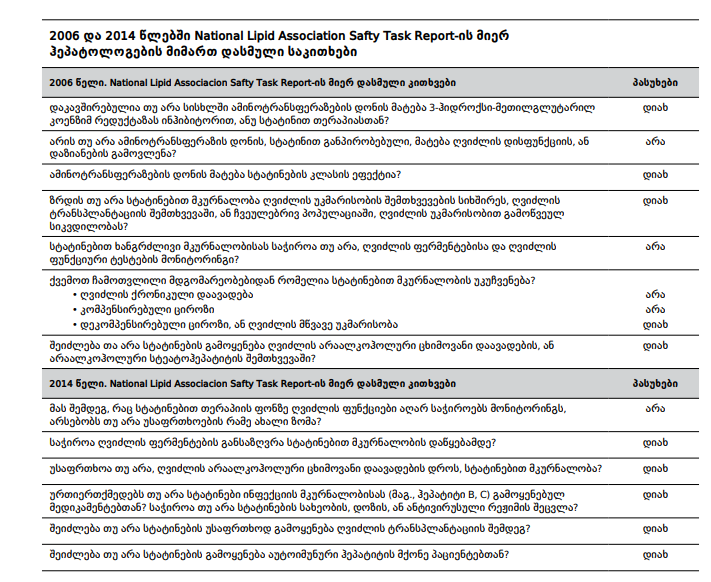
ღვიძლის ფერმენტების მონიტორიგნი
თანამედროვე მონაცემებით, სტატინებით თერაპიისას ღვიძლის ფერმენტების რუტინული მონიტორინგი არ არის რეკომენდებული. მართლაც, რუტინულმა კონტროლმა შესაძლოა გამოავლინოს პაციენტები იზოლირებულად ALT, AST და GGT მატებით და უბიძგოს ექიმებს, საჭიროების გარეშე შეაჩეროს სტატინებით თერაპია, ან შეამციროს დოზა, რაც პაციენტს მნიშვნელოვნად გაუზრდის კარდიოვასკულარული მოვლენების (ინფარქტი და ინსულტი) რისკს. მიზანშეწონილია ღვიძლის ფუნქციების კონტროლი მაშინ, როცა სავარაუდოა ჰეპატოტოქსიკურობის სიმპტომები (მაგ., უჩვეული სისუსტე და დაღლა, მადის დაკარგვა, მუცლის ტკივილი, შარდის გამუქება, ან კანისა და სკლერების გაყვითლება). ასეთ შემთხვევაში, თუკი პაციენტს აქვს ALT ნორმის ზედა ზღვრზე >3-ჯერ მაღალი (ან ნაკლებადაც კი, თუ კომბინირებულია ბილირუბინის მანამდე არსებულ მატებასთან), სტატინებით თერაპია უნდა შეჩერდეს. მხედველობაშია მისაღები სხვა პოტენციური გამომწვევი მიზეზები, სანამ გადაწყდება, რომ ჰეპატოტოქსიკურობა სტატინებითაა ინდუცირებული.
ALT-ის მსუბუქი მატების დროს, რაც განპირობებულია სტეატჰეპატოზითა და ღვიძლის არაალკოჰოლური ცხიმოვანი დაავადებით, სტატინები არ იწვევს ღვიძლის მდგომარეობის გაუარესებას, თუმცა, სიფრთხილით უნდა დაინიშნოს იმ პაციენტებთან, ვისაც აქვს ბილიარული ციროზი. უფრო მეტიც, სტატინებით თერაპიის კარდიოვასკულარული სარგებელი მნიშვნელოვნად გადაწონის ნებისმიერი სახის უსაფრთხოების საკითხს, რაც მკვეთრად ხაზგასმულია გაიდლაინებში. მართლაც, მეტა-ანალიზის მიხედვით, რომელიც მოიცავდა ღვიძლის ქრონიკული დაავადების მქონე 120 000 პაციენტს, სტატინებით თერაპიამ შეამცირა ღვიძლის დეკომპენსაცია და სიკვდილობა და, სავარაუდოდ, პორტული ჰიპერტენზიაც. სტატინები არ უნდა იქნეს დანიშნული მწვავე B ვირუსული ჰეპატიტის დროს ტრანსამინაზებისა და ბილირუბინის ნორმალიზაციამდე.
სტატინების გამოყენებასთან დაკავშირებული დადასტურებული თუ ცრუ გვერდითი ეფექტების გარდა, გამოთქმული იყო მოსაზრება, რომ სტატინებით თერაპია, შესაძლოა, დაკავშირებული იყო დამატებით სხვა გვერდით ეფექტებთანაც (მაგ., ღვიძლის დაზიანება, ძილის დარღვევები, აგრესია, სუიციდური ქცევა, ერექციული დისფუნქცია, ნეიროპათია, კოგნიტური დარღვევები, მეხსიერების გაუარესება, დემენცია, კატარაქტა). ეს ცრურწმენები, როგორც წესი, ეყრდნობოდა ერთეულ შემთხვევებსა და ობსერვაციულ კვლევებს. მეტწილად, ეს დაუსაბუთებელი წარმოდგენები გაქარწყლდა ფართომასშტაბიანი კვლევებიდან მიღებული საკმარისი მტკიცებულებებით.
სტატინებით მკურნალობის სარგებელი/რისკის თანაფარდობა
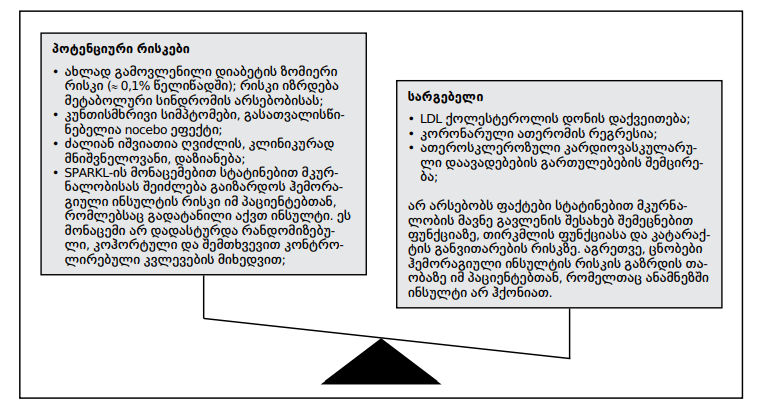
შეჯამება
მნიშვნელოვანია უკეთ გაცნობეიერება იმისა, რომ ობსერვაციულ კვლევებსა და ცალკეული კლინიკური შემთხვევების განხილვას არ აქვს მყარი მტკიცებულება და აღენიშნება მრავალი შეზღუდვა. არ შეიძლება მათი პირდაპირ გადმოტანა და დანერგვა პრაქტიკაში. ამის საპირისპიროდ, მნიშვნელოვანია ადეკვატური მასშტაბის რანდომიზებული კლინიკური კვლევების სიმძლავრისა და მნიშვნელობის უკეთ გააზრება.
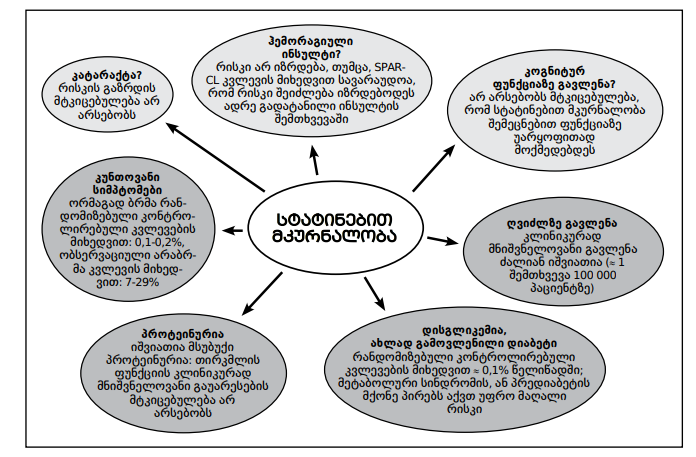
საზოგადოების ცნობადობა სტატინების გვერდითი ეფექტების შესახებ ხშირად გადაჭარბებული და ზოგ შემთხვევაში, ცრურწმენაა, რაც, ნაწილობრივ, მედიით გავრცელებული შემთხვევების შედეგია, მაშინ, როდესაც სტატინებს აქვთ აბსოლუტურად მისაღები უსაფრთხოების პროფილი; ევროპის ათეროსკლეროზის საზოგადოების კომისიამ კიდევ ერთხელ განიხილა განახლებული მტკიცებულებები სტატინების გამოყენების უსაფრთხოების შესახებ. კომისიის შეხვედრისა და საერთო შეთანხმების მიხედვით, სტატინებით თერაპია უსაფრთხოა. შაქრიანი დიაბეტის გამოვლენის სიხშირე 1 შემთხვევაა 1000 პაციენტზე წელიწადში, მაშინ, როდესაც 5 ინფრაქტისა და ინსულტის პრევენცია ხდება. პრედიაბეტისა და მეტაბოლური სინდრომის მქონე პირები მეტად არიან განწყობილი დიაბეტის განვითარებისკენ. სავარაუდოდ, ეს უნდა იყოს კლასის ეფექტი, თუმცა, არ არსებობს head to head კვლევები, რომელიც შეაფასებდა თითოეული სტატინის გავლენას გლუკოზის ჰომეოსტაზზე. დაგროვილ მტკიცებულებებზე დაყრდნობით, დადასტურებულად შეიძლება ითქვას, რომ სტატინებით თერაპიას არ გააჩნია უარყოფითი გავლენა თირკმლისა და კოგნიტურ ფუნქციებზე, არ ზრდის კატარაქტისა და ჰემორაგიული ინსულტების სიხშირეს იმ პაციენტებში, რომლებსაც ადრე ინსულტი არ ჰქონიათ. თუმცა, SPARCL კვლევის მონაცემების მიხედვით, შესაძლოა, სტატინები ზრდის ჰემორაგიული ინსულტების სიხშირეს იმ პაციენტებში, რომლებსაც უკვე გადატანილი აქვთ ინსულტი. სტატინების მიერ ღვიძლის კლინიკურად მნიშვნელოვანი დაზიანება უკიდურესად იშვიათი მოვლენაა. ევროპის ათეროსკლეროზის საზოგადოების მიერ შეჯამების სახით ხაზგასმულია შემდეგი ფაქტი პრაქტიკოსი ექიმებისთვის: „სტატინებით თერაპიის კარდიოვასკულარული სარგებელი მნიშვნელოვნად გადაწონის ნებისმიერი სახის გვერდითი ეფექტის განვითარების რისკს“.
სტატია მომზადებულია ლანცეტში 2016 წელს გამოქვეყნებული იმავე სახელწოდების პუბლიკაციასა და ევროპის ათეროსკლეროზის საზოგადოების მიერ 2018 წელს გამოშვებულ კლინიკურ განახლებაზე დაყრდნობით საქართველოს ენდოკრინოლოგიისა და მეტაბოლიზმის ასოციაციის (GAEM, სემა) მიერ.
წყარო:
European Heart Journal (2018) 0, 1–18 – doi:10.1093/eurheartj/ehy182
Lancet 2016; 388: 2532–61 – Published Online September 8, 2016
